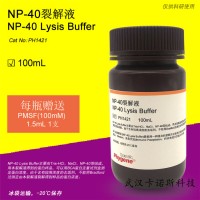
規格 PH1421-100 | 100mL
存儲 冰袋運輸,-20℃保存
有效期:至少12個月
試劑組份
試劑A:NP-40 Lysis Buffer----100ml----Store at -20℃
試劑B:PMSF(100mM)----1.5ml----Store at -20℃
產品簡介
NP-40 Lysis Buffer主要由Tris-HCl、NaCl、NP-40等組成。用本裂解液得到的蛋白樣品,可以用BCA蛋白定量試劑盒測定蛋白濃度。由于含有較高濃度的去垢劑,不能用Bradford法測定由本裂解液裂解得到樣品的蛋白濃度。
NP-40裂解液 (NP-40 Lysis Buffer)是采用一種溫和的裂解方法獲得總蛋白的裂解液。所獲得的蛋白質可以用于PAGE電泳、Western、免疫沉淀(Immunol Precipitation,IP)和免疫共沉淀(co-IP)等。
使用說明
(一)貼壁培養細胞
1.取NP-40 Lysis Buffer 置于室溫溶解混勻,加入PMSF,使PMSF終濃度為1mM。例如取每1ml RIPA 加入10ul PMSF,使PMSF的最終濃度為1mM,混勻備用 (PMSF現用現加)。
2.去除貼壁細胞的培養液,用PBS、NS或無血清培養液清洗1次,低速離心,棄上清,留取沉淀。
3.按照6孔板每孔加入150~250μl含有PMSF的裂解液的比例,加入NP-40 Lysis Buffer 。移液器輕輕吹打,使裂解液和細胞充分接觸。置于冰上或4℃裂解15~30min,通常裂解液作用于細胞1~3s內,細胞就會被裂解。
4.10000~12000g,4℃離心5~10min(如無低溫離心機,室溫下離心亦可),取上清。
5.進行后續的SDS-PAGE、Western、免疫沉淀和免疫共沉淀等操作。
(二)懸浮培養細胞
1.取NP-40 Lysis Buffer 置于室溫溶解混勻,加入PMSF,使PMSF終濃度為1mM。低速離心懸浮細胞,棄上清,收集沉淀。
2.用手指輕彈細胞,使其松散。按照6孔板每孔細胞加入150~200μl含有PMSF的裂解液的比例,加入NP-40 Lysis Buffer。通常6孔板每孔細胞加入150μl裂解液已經足夠,但如果細胞密度非常高可以適當加大裂解液的用量到200~250μl。再用手指輕彈以充分裂解細胞,充分裂解后應沒有明顯的細胞沉淀。
3.10000~12000g,4℃離心5~10min(如無低溫離心機,室溫下離心亦可),取上清。
4.進行后續的SDS-PAGE、Western、免疫沉淀和免疫共沉淀等操作。
(三)組織樣本
1.取NP-40 Lysis Buffer 置于室溫溶解混勻,加入PMSF,使PMSF終濃度為1mM。把組織剪切成細小的碎片,越小越好。
2.取在液氮或超低溫冰箱中冷凍30min以上的組織,迅速用液氮研磨,研磨過程盡量控制在1~2min之內,以減少蛋白的降解。
3.按照每20mg組織加入150~250μl裂解液的比例加入含有PMSF的裂解液。冰上或4℃裂解30~60min。
4.步驟3、4亦可以采用如下過程:按照每20mg組織加入150~250μl裂解液的比例,加入含有PMSF的NP-40 Lysis Buffer。用玻璃勻漿器或組織研磨器勻漿,直至充分裂解,該過程盡量控制在1~2min之內,以減少蛋白的降解。
5.10000~12000g,4℃離心5~15min(如無低溫離心機,室溫下離心亦可),取上清。
6.進行后續的PAGE、Western、免疫沉淀和免疫共沉淀等操作。
注意事項
1)在貼壁培養細胞的操作步驟中,去除貼壁細胞的培養液后,如果血清中的蛋白沒有干擾,可以不用清洗。
2)如果裂解不充分可以適當增加裂解液的用量,如果需要高濃度的蛋白樣品,可以適當減少裂解液的用量。
3)在培養細胞的裂解中,如果細胞量較多,必需分裝成50~100萬細胞/離心管,然后再裂解。大團的細胞較難裂解充分,而少量的細胞由于裂解液容易和細胞充分接觸,相對比較容易裂解充分。
4)如果組織樣品本身非常細小,可以適當剪切后直接加入裂解液裂解,通過強烈Vortex使樣品裂解充分。然后同樣離心取上清,用于后續實驗。直接裂解的優點是比較方便,不必使用勻漿器,缺點是不如使用勻漿器那樣裂解得比較充分。
5)溶解NP-40 Lysis Buffer時,應盡量縮短溶解時間,避免裂解液中的有效成分失效。
6)細胞裂解的操作步驟,應置于冰上或4℃進行。
7)為了您的安全和健康,請穿實驗服并戴一次性手套操作。
*important Note: This product as supplied is intended for research use only, not for use in human, therapeutic or diagnostic applications.





 糠醛 α-呋喃甲醛 CAS98-01-1 用作
¥10.00/kg
糠醛 α-呋喃甲醛 CAS98-01-1 用作
¥10.00/kg
 氧化鐵黃 CAS51274-00-1 湖北廠家生
¥3.00/kg
氧化鐵黃 CAS51274-00-1 湖北廠家生
¥3.00/kg
 乙二胺鹽酸鹽 有機原料 工廠直銷 質
¥3.00/kg
乙二胺鹽酸鹽 有機原料 工廠直銷 質
¥3.00/kg
 水楊酸 醫藥工業生產 生產廠家 現貨
¥8.00/kg
水楊酸 醫藥工業生產 生產廠家 現貨
¥8.00/kg
 -10℃變壓器油 良好的熱安定性 湖北
¥3.00/kg
-10℃變壓器油 良好的熱安定性 湖北
¥3.00/kg
 苯甲酸 CAS65-85-0 廠家直銷 質量保
¥3.00/kg
苯甲酸 CAS65-85-0 廠家直銷 質量保
¥3.00/kg
 苯甲酸鉀 CAS532-32-1 湖北廠家生產
¥3.00/kg
苯甲酸鉀 CAS532-32-1 湖北廠家生產
¥3.00/kg
 AES 脂肪醇醚硫酸鈉 110kg/桶 當天
¥3.00/kg
AES 脂肪醇醚硫酸鈉 110kg/桶 當天
¥3.00/kg
 2-乙酰基吡嗪 CAS22047-25-2 當天發
¥3.00/kg
2-乙酰基吡嗪 CAS22047-25-2 當天發
¥3.00/kg
 醋酸錳 淡紅色針狀晶體 湖北廠家 當
¥6.00/kg
醋酸錳 淡紅色針狀晶體 湖北廠家 當
¥6.00/kg